Calorimetria é
a parte da ciência
física que
estuda as trocas de energia entre
corpos ou sistemas quando essas trocas se dão na forma
de calor.1 Calor
significa uma transferência de energia
térmica de
um sistema para outro, ou seja: podemos dizer que um corpo recebe
calor, mas não que ele possui calor. A Calorimetria é uma
ramificação da termologia.
Termologia
Calor -
Energia térmica que flui de um corpo para outro em virtude da
diferença de temperatura entre eles. Pode ser adicionado ou removido
de uma substância. É medido em calorias ou joulesS.I.
Capacidade
térmica (C) -
É a capacidade de um corpo de mudar sua temperatura ao receber ou
liberar calor. Ela é dada como a razão entre a quantidade de calor
e a variação de temperatura.
- C: capacidade térmica do corpo.
- Q: quantidade de calor trocada pelo corpo.
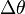 :
variação de temperatura do corpo.
:
variação de temperatura do corpo.
A
unidade de capacidade térmica no S.I. é o J/K (joule por kelvin).
Calor
específico (c):
É a capacidade específica de uma substância de mudar sua
temperatura ao receber ou liberar calor para cada massa unitária que
esta vier a se incluir. Isto quer dizer que a Capacidade Térmica de
um corpo é dada pelo Calor Específico da substância que o compõe
e sua massa.
A
unidade usual para determinar o calor específico é
- c: calor específico de um dado material.
- C: capacidade térmica da amostra deste material.
- M: massa da amostra deste material.
Uma
caloria (1 cal): é a quantidade de calor necessária para aquecer,
sob pressão normal, 1,0 g de água de 14,5°C a 15,5°C.
Função
Fundamental da Calorimetria (Quantidade de Calor Sensível)
Ocorre
mudança de temperatura nas substâncias.
- Q>0 (o corpo recebe calor)
 (o
corpo se aquece).
(o
corpo se aquece). - Q<0
(o corpo cede calor)
 (o
corpo se esfria).
(o
corpo se esfria).
Experiência com balões:
Material: 5 balões, 5 garrafas PET, Bicarbonato de sódio, funil, vinagre
Procedimentos:
- Coloque a quantidade de vinagre de uma tampa em cada garrafa conforme a indicação:
1 - 3- 7 - 10 - 13
- Coloque a mesma quantidade de Bicarbonato de sódio uma tampinha dentro de cada balão e fixe cada balão na boca da garrafa.
- Em seguida vire o Bicarbonato de sódio dos balões dentro das garrafas e observe o que acontece.




Nenhum comentário:
Postar um comentário